ARTÍCULOS ORIGINALES
EFICACIA DE IgY ANTI-ROTAVIRUS VÍA ORAL EN EL TRATAMIENTO DE DIARREAS
AGUDAS POR ROTAVIRUS
EFFECTIVENESS ROTAVIRUS IgY MOUTH IN THE TREATMENT OF ACUTE DIARRHEA ROTAVIRUS.
Carlos Enrique Azabache Diaz 1
Noelle Isabel Anticona Carranza
2
RESUMEN
Con el propósito de determinar la eficacia de la
Inmnoglobulina Y antoritavirus en el tratamiento de la diarrea acuosa por
Rotavirus. Se realizó un ensayo clínico en 230 niños, divididos en dos
grupos estudio, 115 niños quienes se les administro Inmunoglobulina
Y (Grupo 1), y 115 niños que
conformaron el grupo control (Grupo2), los pacientes fueron
atendidos desde Junio del 2005 hasta febrero del 2006 en la Clínica Anticona
localizada en Trujillo - Perú. Se encontró predomino del sexo femenino
(>50%) en ambos grupos, antecedente de rinofaringitis aguda (>90%) en
ambos grupos, deshidratación en el 100% del grupo de estudio. Con relación a
las manifestaciones clínicas: vómitos, fiebre, deshidratación y episodios de
diarrea por día, los cambios
fueron
cuantitativamente mayores y estadísticamente diferentes
a favor del grupo de estudio; se observó una media de 1.58 días de duración de
la enfermedad después del tratamiento en el grupo de estudio, comparada
con una media de 3.54 días en el grupo control (p<0.01). Concluyéndose que
la IgY antirotavirus vía oral es eficaz en el Tratamiento de diarreas agudas
por Rotavirus.
Palabras Claves: Diarrea
por Rotavirus, Inmunoglobulina Y antirotavirus.
ABSTRACT
In order to determine the effectiveness of Inmnoglobulina Y antoritavirus in the treatment of watery diarrhea rotavirus. We performed a clinical trial in 230 children, divided into two groups study, 115 children who were administered immunoglobulin Y (Group 1), and 115 children who comprised the control group (Group 2), patients were treated from June 2005 until February 2006 in Anticona Clinic located in Trujillo - Peru. We found a predominance of females (> 50%) in both groups, history of acute nasopharyngitis (> 90%) in both groups, dehydration in 100% of the study group. With regard to clinical manifestations: vomiting, fever, dehydration, and episodes of diarrhea per day, the changes were quantitatively greater and statistically different in favor of the study group, we found an average of 1.58 days of duration of disease after treatment the study group, compared with an average of 3.54 days in the control group (p <0.01). Concluding that the oral rotavirus IgY is effective in the treatment of acute rotavirus diarrhea.
Key words: Rotavirus diarrhea, and rotavirus immunoglobulin.
INTRODUCCIÓN
Las diarreas
agudas son uno de los cuadros clínicos más comunes entre niños de 0 y 5 años.
En líneas generales, la diarrea impide que el cuerpo procese y absorba el agua
necesaria, sales y elementos nutritivos, lo que puede llevar a diversos grados
de deshidratación y hasta la muerte. En el Perú representa alrededor de 385 mil
casos y 1.600 defunciones por año, por lo constituye un problema de Salud
publica (1,2).
Dentro de la
etiología de este cuadro clínico, los Rotavirus constituye la causa más
frecuente, siendo su frecuencia entre el 70-80% de los casos. Su distribución geográfica
es universal y pueden ser más frecuentes en las regiones socioeconómicas más
pobres (3-5). En los países desarrollados, los Rotavirus constituyen el agente
único más frecuente de diarrea en los niños menores de 2 años que necesitan
asistencia médica, concentrándose el mayor número de casos entre los 3-12 meses
de edad, con un claro predominio en los meses invernales.
Rotavirus es
también la causa más frecuente de hospitalización y deshidratación,
afectando aproximadamente al 50% de los ingresos y causando la muerte por
deshidratación en el 0,75% de los niños menores de 2 años afectados, se estima
que alrededor del 60% de los niños
al cumplir los 5 años de edad habrá
presentado al menos un episodio de enfermedad diarreica asociada a
rotavirus (6,7).
La
transmisión de este virus es exclusivamente
por vía fecal-oral, La transmisión está
asociada a la falta de higiene y
en ciertos casos aumenta especialmente en la época de
verano. Se acentúa más en las zonas que no cuentan con una infraestructura de
saneamiento ambiental adecuada, lugares que pueden incluso ser foco de
infección para los más pequeños. La infección puede ser asintomática pero puede
desencadenar en enfermedad, presentándose en este caso como un simple malestar
estomacal con fiebre, vómitos y diarrea de grado diverso que va de leve a grave
con compromiso vital (8-10).
Se
han desarrollo varios estudios dirigidos a
la prevención de esta enfermedad, las vacunas que
existen es prueba de ello. Sin embargo, actualmente, su
costo no esta acorde con el poder
adquisitivo de nuestra población, específicamente
del estrato socioeconómico bajo en donde
esta enfermedad es mas frecuente(6).
Una alternativa a
este problema, es la administración de Inmunoglobulina
antirotavirus en Yema de huevo en polvo (IgY antirotavirus),
Tecnología desarrollada por Biondist CO. LTD, sustancia que puede ser ingerida
sola o mezclada con alimentos del niño. Además de su bajo costo comparado con las
vacunas que existen, es una ventaja adicional. Won-Yong en el año 2002, realizó
un ensayo clínico en 40 niños con diarrea causada por rotavirus,
administrándole Yema de huevo en polvo (IgY antirotavirus), valorando, por 3
días consecutivos, la sintomatología y la identificación de la cepa de
rotavirus en heces; encontró que el 66% presentó una disminución entre 34.7% y
46.3% de la cepa del rotavirus y menor frecuencia de sintomatología con
asociación estadística, demostrando la utilidad de esta sustancia (11).
La prevención de
las diarreas agudas es una actividad que compromete a todo el
personal de salud y teniendo en
cuenta lo expuesto, formulamos el siguiente
problema: ¿Es Eficaz la IgY antirotavirus vía oral en el Tratamiento de
diarreas agudas por Rotavirus?, teniendo como objetivo demostrar que el
Uso IgY antirotavirus vía oral es eficaz en el tratamiento de diarreas agudas
por Rotavirus..
MATERIAL Y
MÉTODOS
El universo
estuvo constituido por todos
los
niños con diagnostico clínico de diarrea aguda por Rotavirus atendidos en le
“Clínica Anticona” desde Junio del 2005 hasta febrero del 2006. Los criterios
de inclusión fueron: Todos los niños < 5 años y que sus apoderados hayan
firmado el Consentimiento Informado(A- I); Que presenten Deshidratación leve o
moderada. Los Criterios de exclusión: Niños con enfermedad gastrointestinal
subyacente, niños con Intolerancia oral, niños con desnutrición crónica y
aguda. Los criterios de retiro: Pacientes que abandonan voluntariamente el
estudio.
Para
obtener la muestra se utilizó la
formula para la comparación de 2 proporciones,
nuestro nivel de riesgo lo fijamos en 0.05 y deseamos un poder estadístico de
un 95%.donde P1 y P2 son valores de referencia.
En el cálculo de
la muestra se reportó en cada grupo de estudio 115 pacientes.
El presente
estudio es un Ensayo Clínico Controlado, es un diseño experimental clásico, con
grupo control histórico, con un pretest y varios postest. Grupo 1(G1):
Pacientes a quienes se les administró IgY antirotavirus vía oral. Grupo 2 (G2):
Pacientes sin tratamiento específico.
Para el Grupo de
estudio se administro 2g/ día de IgY antirotavirus vía Oral como tratamiento
especifico. Para el seguimiento de los pacientes, una vez captado el paciente y
realizada la administración de las Ig Y antirotavirus, se realizaron
observaciones diarias durante 7 días consecutivos de tratamiento completo.
Estas mediciones se realizaran personalmente evaluando clínicamente al paciente
de manera ambulatoria. Simultáneamente los datos se registraron en un protocolo
de recolección de datos elaborado para el presente estudio. Los datos
recolectados fueron pre y post a la administración de IgY antirotavirus y datos
referentes a los datos del cuadro clínico: vómitos fiebre, deshidratación,
severidad del mismo (nivel de deshidratación), así como la aparición de los
efectos colaterales después de la administración de la sustancia. Los
puntos finales primarios Fueron: Vómitos, Fiebre, deshidratación y episodios de
diarrea por día.
Con
respecto a los términos utilizados
definimos como Diarrea por Rotavirus, cuando
la clínica consiste en vómitos y
fiebre durante 5-8 días seguidos de
diarrea, además del antecedente de rinofaringitis
aguda en días previos. Afecta con frecuencia a lactantes y niños
menores de 5 años, ocurriendo de forma epidémica durante los meses de verano,
excepto en el recién nacido en quien no parecen existir variaciones
estaciónales. Puede asociarse deshidratación severa con pronóstico vital
precario (5).
El término
Eficacia: quiere indicar que el tratamiento reduce, en el grupo de estudio, la
probabilidad o el riesgo de experimentar un desenlace adverso o grado en que un
tratamiento produce un efecto beneficioso cuando se valora bajo las condiciones
ideales de una investigación. La eficacia es el tratamiento lo que la causa
contribuyente es a la etiología de la enfermedad (12).
Para el presente
trabajo se elaboró una base de datos en el Software estadístico SPSS versión
11, utilizando la prueba “x2” para determinar diferencia significativa entre
ambos grupos y se calculó el CC para cada criterio de evaluación.
RESULTADOS
Gráfico Nº 1: Distribución de la población según sexo
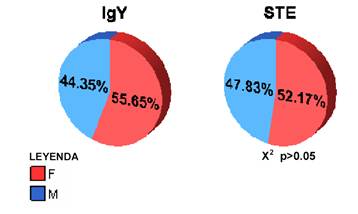
Tabla 1: Medias de la edad según tratamiento
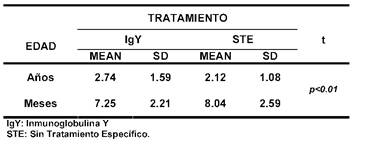
Tabla 2: Distribución de la población según nivel de
deshidratación y tratamiento
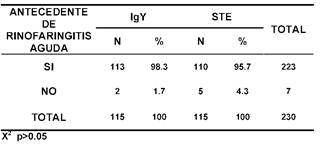
Gráfico 2: Diagrama resumen: vómitos, fiebre, deshidratación y
episodios de diarreas al día antes y después del tratamiento
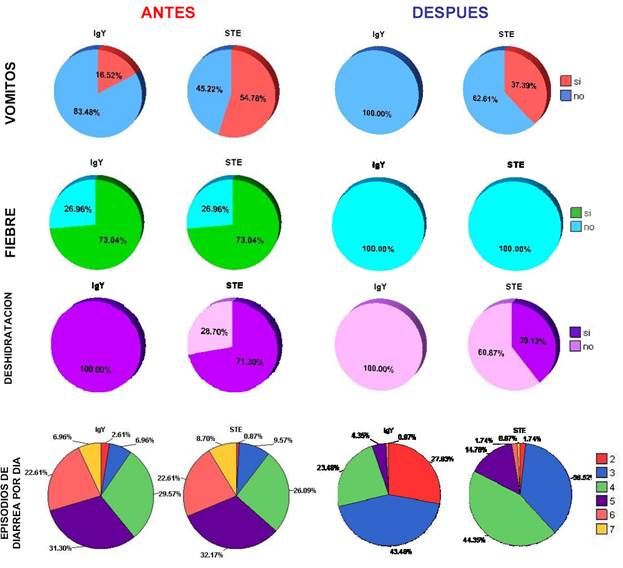
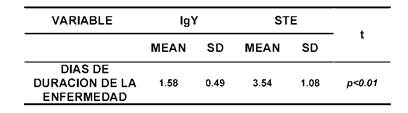
Tabla 3: Media de días de duración de la enfermedad en ambos
grupos
DISCUSIÓN
El estudio se diseñó para determinar la
eficacia de la IgY antirotavirus en el tratamiento de la diarrea acuosa por
rotavirus en niños menores de 5 años, para lo cual se estudió una muestra de
230 niños, divididos en 2 grupos, evaluados en la “Clínica Anticona” de
Trujillo - Perú, el grupo control fue obtenido de los registros de emergencia
del Hospital Regional Docente de Trujillo, es oportuno mencionar que la razón
de aplicar este diseño se debe a que dentro del intervalo de tiempo
empleado para la realización de esta
investigación existieron los siguientes inconvenientes:
la falta de participación de la
comunidad en este estudio, disminución de la incidencia de
esta enfermedad y la falta un examen laboratorial a bajo costo para el primer
grupo. Los criterios de evaluación empleados fueron la variabilidad del Peso
corporal, Episodios de Vómitos y de Diarrea.
En el Gráfico 1 se observa la distribución de
la población de estudio según sexo, que muestra predominio del sexo femenino en
ambos grupos, sin diferencia estadística significativa (p>0.05), en los
estudios publicados con respecto a la infección por Rotavirus, la variable sexo
no es considerada, por lo tanto en el presente estudio este hallazgo se
considera incidental. Sin embargo es una característica similar para comparar
ambos grupos.
Con relación a la edad, en el Cuadro 1, se
observa la comparación de la media de la edad en ambos grupos con predominio de
niños menores de 1 año en el grupo control con diferencia altamente
significativa, similar a lo reportado por Mota y col (13).
La mayor frecuencia de infecciones
sintomáticas por rotavirus fue entre los seis y los 11 meses de edad, siendo
más frecuentes los niños menores de seis meses, estudios prospectivos han
demostrado que entre 15 y 40% de los niños menores de un año sufren infecciones
sintomáticas por rotavirus, mientras que otro 5% a 20% de los niños
experimentan infecciones clínicas durante el segundo año de vida.
En el Cuadro 2, se muestra el antecedente de
Rinofaringitis aguda antes del inicio de la enfermedad diarreica, el cual
estuvo presente en ambos grupos, sin diferencia estadística significativa. Este
antecedente es parte de la historia natural de la enfermedad y hace estos dos
grupos comparables. En el Cuadro 3, se muestra la distribución de la población
según nivel de deshidratación, se observa que en grupo de estudio todos
los niños tuvieron algún nivel de deshidratación mientras que en el grupo
control estuvo ausente en el 28.7%, con diferencia estadística
significativa. La deshidratación es un
signo frecuente en esta enfermedad, estudios previos
reportan que el cuadro clínico incluye, además de presentar
diarrea, presentan otros síntomas: fiebre
(77,3%), vómitos (86,4%), hiporexia (81,8%),
irritabilidad
(9,1%) y deshidratación leve-moderada (63,6% y 59,1%), en algunos
casos hubo la necesidad de hospitalización
[9-11]. En el presente estudio el grupo de estudio el 100% presentó
deshidratación.
En el diagrama resumen Gráfico 2, muestra los
cambios de las manifestaciones clínicas de la enfermedad, antes y después del
tratamiento, se observa según: presencia de vómitos, fiebre y deshidratación,
las modificación son cuantitativamente mayores en el grupo que recibió IgY en
comparación al grupo sin tratamiento especifico, sin embargo el control de
estas manifestación clínicas son resueltas con medidas
generales aplicadas de manera similar en
ambos grupos.
Además, se reporta una asociación encontrada
entre fiebre y deshidratación que pudiera ser explicada en ambos sentidos:
la fiebre contribuye a la aparición de deshidratación o la deshidratación, por
si misma, incrementa la temperatura corporal (14); se requieren otros estudios
para aclarar esta posible interrelación. Con respecto al numero de evacuaciones
al día, se observa un disminución cuantitativamente mayor en el grupo tratado
con IgY, reforzando la utilidad de esta sustancia en el tratamiento de esta
enfermedad. Cabe señalar que se realizó el cálculo del coeficiente de
correlación siendo para ambos grupos positivo.
En el Cuadro 4, muestra la media de duración
de la enfermedad después de la intervención o administración del tratamiento
específico (IgY), se observa una media de 1.58 días en el grupo de estudio,
comparada con una media de 3.54 días en el grupo control, con una diferencia
altamente significativa. Hay que tener en cuenta que
ambos grupos recibieron medidas generales
y tratamiento sintomático, que pueden explicar la solución de
alguna manifestación de forma similar (Fiebre-Grafico 2), pero la disminución
de los episodios de diarreas y la duración de la enfermedad después del
tratamiento difieren estadísticamente a favor del grupo que recibió IgY.
Aunque, Una de las limitaciones de la
presente investigación fue la de no haber realizado estudios
microbiológicos, para demostrar asociación con otros enteropatógenos y
teniendo en cuenta que la efectividad de la hidratación oral para prevenir y
tratar la deshidratación por diarrea ha permitido cuestionar el
costo-beneficio de la aplicación de la
vacuna contra rotavirus como principal intervención en
este problema de salud. Nos Obliga a desarrollar estudios costo – efectividad
del tratamiento de esta enfermedad con IgY.
CONCLUSIÓN
·
Finalmente, los resultados obtenidos en el
presente estudio demuestran que la IgY vía oral
es eficaz en el tratamiento de las
diarreas agudas por Rotavirus.
REFERENCIAS BIBLIOGRÁFICAS
1. Akinci A, Tezic T, Gur I, Cetin H, Hatun S. Rotavirus diarrhoea in newborn infants. Turk J Pediatr 1991; 33:153-7.
2. Bern C, Martines J, de Zoysa I, Glass RI. The magnitude of the global problem of diarrhoeal disease: a ten year update. Bull World Health Organ. 1992; 70:705-14.
3. Bryden AS, Thouless ME, Hall CJ, Flewett TH, Wharton BA, Mathew PM, Craig I. Rotavirus infections in a special-care baby unit. J Infect 1982; 4:43-8.
4. Chrystie IL, Totterdell BM, Banatvala JE. Asymptomatic endemic rotavirus infections in the newborn. Lancet 1978; 1:1176-8.
5. Cicirello HG, Das BK, Gupta A, Bhan MK, Gentsch JR, Kumar R, Glass RI. High prevalence of rotavirus infection among neonates born at hospitals in Delhi, India: predisposition of newborns for infection with unusual rotavirus. Pediatr Infect Dis J 1994; 13:720-4.
6. Guarino A, Canani RB, Russo S, Albano F, Canani MB, Ruggeri FM, Donelli G, Rubino A. Oral immunoglobulins for treatment of acute rotaviral gastroenteritis. Pediatrics 1994;93:12-6.
7. Molyneaux PJ. Human immunity to rotavirus. J Med Microbiol 1995;43:397-404.
8. Turner RB, Kelsey DK. Passive immunization for prevention of rotavirus illness in healthy infants. Pediatr Infect Dis J 1993;12:718-22.
9. Valmari P, Pontynen S, Sunila R. Rotavirus infection in a neonatal unit. Ann Clin Res 1984;16:167-70.
10. Walther F, Bruggeman C, Daniels-Bosman MS. Rotavirus infections in high-risk neonates. J Hosp Infect 1984; 5:438-43.
11. Won-Yong K. Clinical Trial of Chicken Egg Yolk Inmunoglobulin (IgY) in Children with diarrhea caused by Rotavirus (The decrease effect of IgY on rotavirus infected human patient). Department of Microbiology, College of Medicine. ChungAng University. Seoul Korea 2002.
12.
Riegelman RK, Hirsch RP.
Estudios de intervención: ensayos clínicos
controlados. En Riegelman RK, Hirsch RP: Cómo estudiar un estudio y
probar una prueba: lectura crítica de la literatura médica. Washington: OPS.
1992;67-85
13.
Mota H, Gutiérrez C, Villa C, Calva M, Aias
F, Padilla N, Guiscafré G. Pronóstico de la diarrea por rotavirus. Salud
Pública de México. Vol.43, N° 6, 2001: 524-28.
14. Dagan R, Bar-David Y, Sarov B, Katz M, Kassis I, Greenberg D et al. Rotavirus diarrhea in Jewish and Bedouin children in the Negev region of Israel: Epidemiology, clinical aspects and possible role of malnutrition in severity of illness. Pediatr Infect Dis J 1990;9:314-321.
|
Recibido: 11/01/2011 |
Aceptado: 04/02/2011 |
___________________________________________________________________________________________________________________________
1. Médico. Docente de la Carrera profesional Obstetricia.
Universidad Privada Antenor Orrego. Medico Asistente Clínica Anticona- Trujillo.
2. Médico. Universidad Privada Antenor Orrego.